作为中枢神经系统中表达量最高的G蛋白偶联受体(GPCR)之一,大麻素受体CB1参与了包括情绪调节、食欲和脂质代谢、认知功能、伤害感受以及细胞生长和增殖等诸多生物过程,是治疗包括焦虑、肥胖、疼痛和神经退行性疾病等在内的多种疾病的潜在药物靶点。靶向CB1正构位点(orthosteric site)的药物分子,由于可能导致的脱敏、耐受和行为等方面的副作用,其临床用途,特别是在长期药物治疗过程中,往往会受到限制。例如,首个用于治疗肥胖症的CB1特异性拮抗剂利莫那班(2006年)获得欧洲医学委员会(EMA)的上市批准,但却很快因潜在的焦虑、抑郁、自杀倾向等精神方面的副作用被禁止使用。
靶向CB1变构结合位点(allosteric site)的药物提供了一种调节CB1的新方法,可实现同种受体亚型和下游信号通路的选择性调节效应,为更长效且低副作用特征的药物提供可能。因此,CB1变构药物成为人们一直追求的目标,但CB1变构调节的具体分子机制尚不清楚,严重地阻碍了变构药物的研发。

近日,四川大学华西医院生物治疗国家重点实验室杨胜勇教授团队和邵振华研究员团队合作,共同在Nature Chemical Biology杂志在线发表了最新的研究成果“Molecular mechanism of allosteric modulation for the cannabinoid receptor CB1”,在CB1变构调节机制研究领域取得重大进展。该研究成功解析了CB1与正向变构调节剂(positive allosteric modulator, PAM)ZCZ011(图1a-b)的晶体结构(图1c)以及下游信号转导分子Gi蛋白三元复合物的冷冻电镜结构(图1d),利用分子动力学模拟系统阐明了CB1区别于其余class A GPCRs的独特激活以及变构调节机制,揭示了CB1受体从失活态到活化态的激活过程中的关键中间态构象和自由能变化(图2),首次发现TM2在GPCR活化以及变构信号传导中的重要作用,为基于结构的CB1变构调节剂设计提供了重要线索和思路。
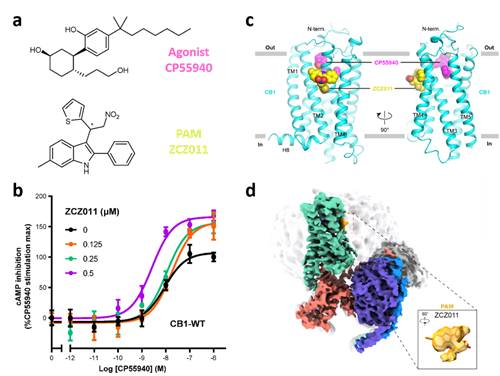
图1. CB1-配体(正构激动剂CP55940和PAM ZCZ011)的X-射线衍射和冷冻电镜结构
晶体与冷冻电镜结构模型表明,ZCZ011分子结合在位于CB1受体TM2-TM3-TM4胞外侧的一个全新的结合口袋中(图1c-d)。这一口袋靠近正位配体结合口袋,距离受体胞质侧下游信号蛋白结合位点较远。为了进一步解释ZCZ011调控CB1及其下游信号的分子机制,研究团队通过定点突变以及信号转导实验方法(图1b),探索了ZCZ011分子与CB1相互作用的结合模式,并通过比较非激活态与激活态的CB1,发现了CB1的TM2在两者状态之间显著的构象变化。这可能与ZCZ011调控CB1相关,并且该变化较少地发生在其他class A类的GPCR中。
为了进一步从动态的原子水平解释CB1的激活机制以及不同变构调节剂调节CB1的微观过程,研究团队应用分子动力学模拟、自由能计算等分子模拟方法对CB1与多种小分子配体之间的相互作用机理以及变构调节势能面进行了系统研究。结果表明,CB1上的TM2构象改变对CB1的激活以及变构调节信号的转导至关重要(图2a)。当只有激动剂CP55940结合在CB1正构位点上时,势能面(图2b)清晰地显示非活化/活化构象之间的转变涉及到TM2胞内段的旋转以及TM6的外移,其中能垒最高的步骤对应着F1552.42构象的改变(从F1552.42-in改变为F1552.42-out)和由此产生的TM2的重排。激活势能面中所发现的F1552.42对CB1活化的重要性进一步在点突变实验中得到了验证(图2c): 与野生型受体相比,F1552.42突变为侧链较大的色氨酸(F1552.42W)可降低激动剂诱导的受体激活,而突变为侧链较小的缬氨酸(F1552.42V)可增强Gi信号传导能力。
PAM ZCZ011的结合,一方面,导致结合口袋处残基的重排,促进了TM2重排,从而有利于CB1的激活(图2d)。另一方面,ZCZ011与TM3中已向上移动的F1913.27形成氢键以及π-π相互作用,从而稳定TM3上移(upward movement)后的构象,有助于稳定CB1的活化状态。与PAM ZCZ011的结合所带来的促进CB1活化所不同的是,NAM ORG27569在TM2-TM3-TM4胞外侧的结合却因阻碍TM2的重排而诱导受体产生相反的变构调节作用(图2e)。总之,本研究首次揭示了TM2重排在CB1活化和变构调节中的重要作用,可用于指导CB1变构调节剂的设计。
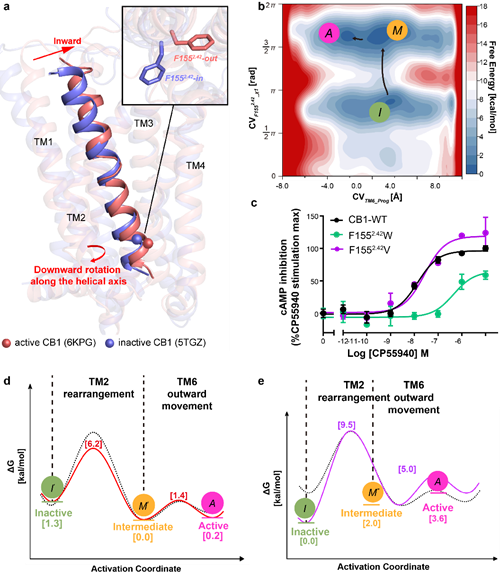
图2.分子动力学模拟揭示了CB1的变构调节机制
四川大学华西医院为本课题第一完成单位和第一通讯单位,副研究员杨欣、博士研究生王学辉、博士后徐政以及博士研究生吴超为本文共同第一作者;杨胜勇教授和邵振华研究员为共同通讯作者。感谢四川大学华西冷冻电镜平台及四川大学华西医院WCH-BDP大数据平台对本项目的支持。该工作在国家自然基金委重点项目、四川大学华西医院1·3·5计划项目等的经费支持下完成。
杨胜勇教授团队长期从事分子模拟与药物分子设计、以及针对重大疾病的小分子靶向药物研发等工作。研究成果以通讯作者发表于Science、Nat Microbiol、Nat Chem Biol、Chem Rev、Angew Chem Int Ed、J Med Chem等本领域重要期刊。邵振华研究员团队长期从事药物靶标GPCR信号转导的结构药理学研究,发现了多个GPCR的变构调控位点。研究成果以通讯作者发表于Cell、Cell Res、Nat Chem Biol、Nat Commun等国际期刊。
原文链接:https://www.nature.com/articles/s41589-022-01038-y