近日,我校华西医院超声医学科邱逦教授医工交叉学科研究团队在材料领域知名期刊Advanced Materials发表了题为“Modulating Electron Transfer in Vanadium-based Artificial Enzymes for Enhanced ROS-Catalysis and Disinfection”的封面论文(图 1)。该论文揭示了一种利用独特的Zn-O-V桥构筑钒基的新型HPO人造酶材料,并验证其具有与万古霉素相当的抗菌性能,能够有效促进创面新生血管形成、降低组织修复过程中的炎性反应,为人工酶的设计提供新的研究思路。我校华西医院超声医学科博士研究生李玲、专职博士后曹素娇为该论文共同第一作者,华西医院超声医学科邱逦教授、高分子科学与工程学院程冲研究员为该论文的共同通讯作者,华西医院为第一作者单位。

图1 杂志封面
自然界的天然酶催化各种生化反应,使生物系统能够适应复杂的环境变化。其中,天然HPO酶广泛存在于自然界,维持生命活动及产ROS杀灭病原体等。近年来,模拟天然酶生物催化活性和功能的人造酶材料越来越受到研究人员的关注。目前具有类HPO酶活性的人工酶在疾病诊疗的研究已取得很大进展。然而,由于对人工酶催化活性中心电子结构的认识不足以及对ROS产生机制的不确定性,大多数已开发的仿HPO人造酶材料的生物催化活性往往较低,亟待研发新型催化材料结构来模拟HPO酶活性位点。
邱逦教授团队首次提出利用独特的Zn-O-V桥调节酶的催化活性中心d电子偏移、提高人工酶催化性能这一理论,并设计研发了一种基于钒基的新型人工酶(VOx-AE)(图2)。该酶具有类似于天然HPO酶的催化活性中心(Zn-O-V桥),在有H2O2存在的条件下实现高效产ROS。研究人员通过显色反应、荧光标记物等方法检测到VOx-AE具有产多种自由基的性能(图 3),在有Cl-存在时,还能实现产次氯酸。通过酶动力学参数分析VOx-AE的Vmax是V2O5的2倍,TON是V2O5的3倍。研究人员还进一步利用抗耐药菌及促创面愈合实验,验证了该人造酶材料高效产ROS仿生催化性能。抗菌实验发现,VOx-AE产生的大量ROS可造成细菌膜过氧化,改变细菌膜的通透性,最终破坏细菌膜实现高效抗菌。动物实验结果表明,VOx-AE的抗菌效果及促进创面愈合速度与万古霉素相当,可有效促进创面血管形成、降低组织修复过程中的炎性反应(图 4)。
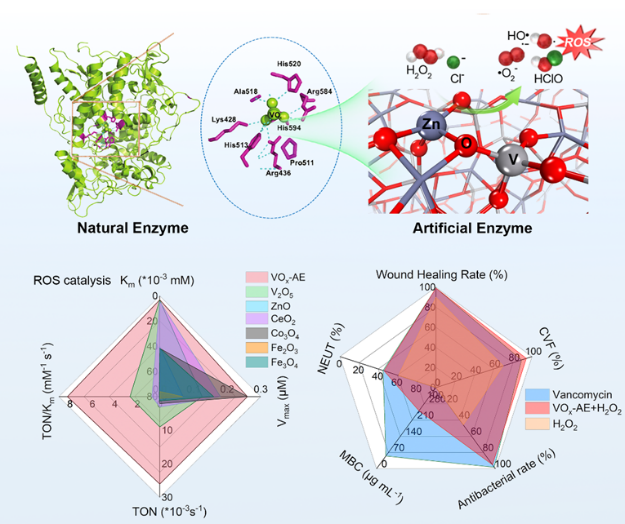
图2 VOx-AE具有类似于天然酶HPO酶的活性中心
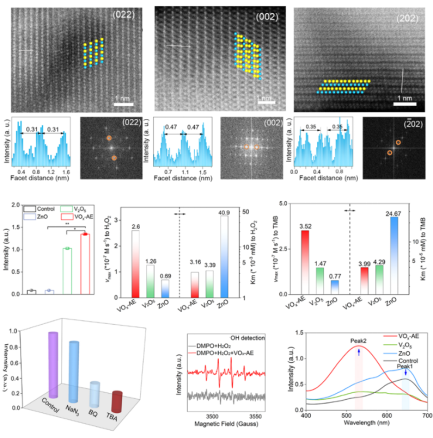
图3 VOx-AE的原子结构,高效的催化性能和产多种自由基的能力
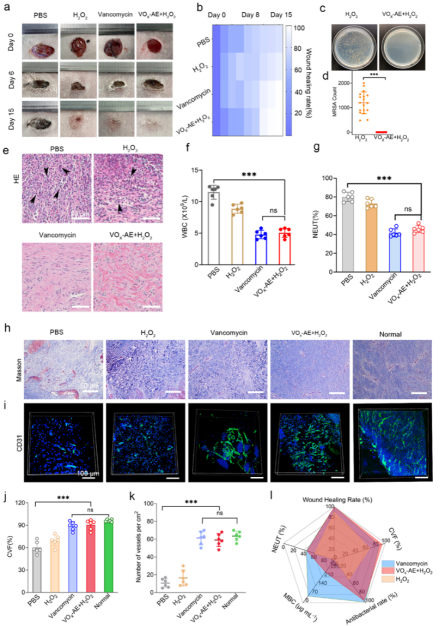
图4 能有效实现抗菌并促进伤口愈合
研究人员还从电子密度差异和Bader电荷分析比较了人工酶VOx-AE和V2O5的催化性能(图5),认为是VOx-AE的催化活性中心(Zn-O-V桥)的bader电荷高于V2O5,使Zn的电子通过Zn-O-V桥向V发生偏移,使V周围的电子增多,催化活性增强。本研究还首次用dyz电子轨道的费米能级来分析VOx-AE的催化活性。该研究理论可为人工酶的设计提供新的研究思路(图6)。
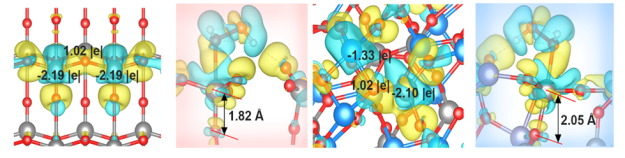
图5 催化产ROS活性的路径及理论分析
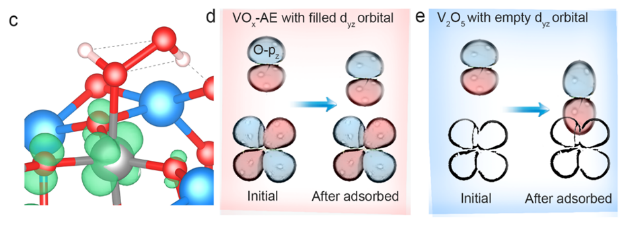
图6 VOx-AE和V2O5的电子结构分析
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202108646